Avec de faux embryons, comment des chercheurs espèrent traiter l'infertilité
SCIENCES - Des travaux qui pourraient avoir un impact de taille sur le monde de l’infertilité. La revue Nature publie ce jeudi 2 décembre une étude promettant d’augurer la création d’un nouveau paradigme pour la fertilité et la contraception.
Cette étude, nous la devons à l’équipe du Français Nicolas Rivron, qui officie à l’Institut de biologie moléculaire de l’Académie des sciences de Vienne. Nous avons pu nous entretenir avec lui à l’aube de cette publication.
Il nous a raconté être parti de l’idée que l’étude des embryons humains était très parcellaire, pour des raisons éthiques et pratiques. Or, “il se passe beaucoup de choses dans les premiers jours après la fertilisation, explique Nicolas Rivron, qui ont un impact très important sur le devenir de l’embryon.”
Ces travaux pourraient justement nous permettre de percer les mystères des premiers jours de l’embryon.

L’enjeu, c’est l’implantation de l’embryon
“Par exemple, nous savons que 50% des fertilisations ne donnent pas de bébé, c’est-à-dire qu’elles se transforment en fausses couches. Et parmi ces 50%, il y a 75% de ces embryons qui ne réussissent pas à s’implanter dans l’endomètre.” L’endomètre est la muqueuse qui tapisse l’intérieur de l’utérus et le lieu de la grossesse.
“L’implantation est un moment critique, très difficile à passer, notamment pour les couples infertiles.” De plus, une mauvaise implantation a un impact sur la taille du bébé, qui risque d’être plus petite, donc engendrer un risque plus important de développer des problèmes cardio-vasculaires bien après.
Donc l’implantation est l’une des clés de l’infertilité. Mais comment l’améliorer si on ne peut pas travailler sur les embryons et leur nidation dans l’utérus? Il y a quelque chose d’ubuesque dans cette situation. En 2019, l’Inserm estimait ainsi qu’“un couple sur huit consulte en raison de difficultés à avoir un enfant.”
La création des blastoïdes
“Il nous faut des alternatives pour comprendre tous ces mécanismes, assure Nicolas Rivron. En 2018, nous avons proposé de former des modèles d’embryons en laboratoire à partir de cellules souches chez la souris et nous avons obtenu un modèle complet. Nous l’avons transféré dans des utérus de souris pour étudier le procédé d’implantation. En 2021, nous proposons le modèle de blastoïde équivalent chez l’humain.”
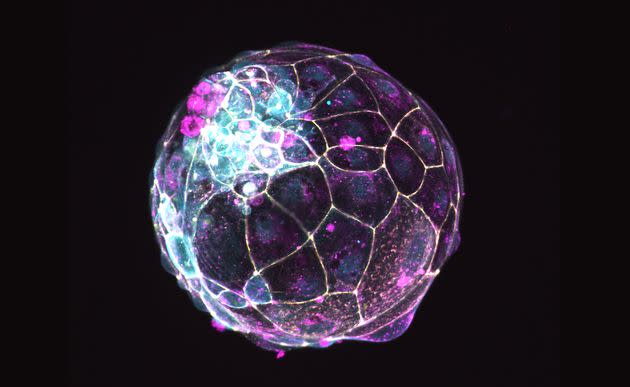
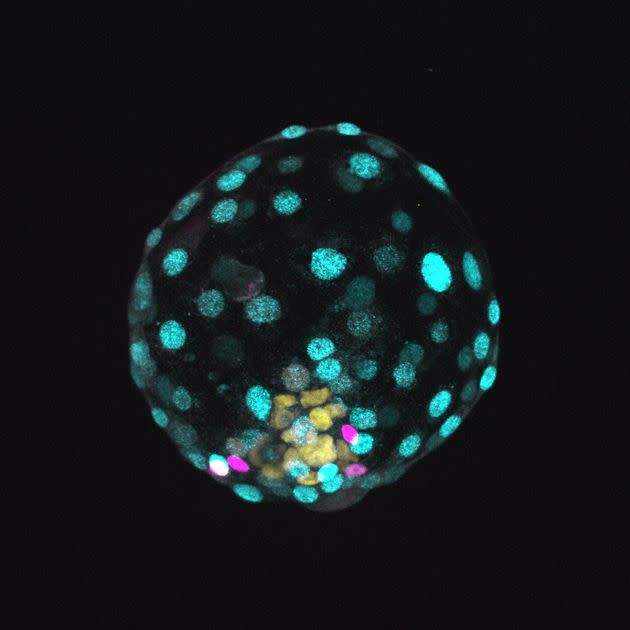
“Nous avons appelé ces embryons des ‘blastoïdes’, pour bien faire la différence avec les blastocytes, les embryons humains, naturellement formés, composés d’une centaine de cellules, sans aucun organe ni membre, de l’épaisseur d’un cheveu.”
Ainsi, les blastoïdes sont des modèles formés en laboratoire et les blastocytes sont des embryons humains. En d’autres termes, ils sont de faux embryons humains, et ils en représentent une structure équivalente.
Créer un cadre éthique nouveau
D’autres études émanant d’équipes américaines, australiennes et allemandes, parues dans le courant de l’année 2021, souvent dans Nature, démontrent tout l’intérêt de ces blastoïdes.
Mais ceux-ci ont aussi déjà suscité des interrogations éthiques. “Avec cette nouvelle catégorie d’objets vivants créés par l’être humain, nous sommes dans une zone grise”, estime ainsi Hervé Chneiweiss, président du comité d’éthique de l’Inserm, contacté par Le Monde.
À ce titre, Nicolas Rivron se montre rassurant. “Évidemment, pour ce type de recherches, continue-t-il, nous avons eu besoin de construire un cadre éthique. Nous nous sommes adressés à la Société internationale pour la recherche sur les cellules souches. Grâce à elle, nous avons publié le premier cadre éthique pour la recherche sur les blastoïdes. Dès lors, ce cadre interdit que les blastoïdes humains soient transférés dans l’utérus humain ou animal.”
Reste à assurer le fonctionnement des blastoïdes, qui doit ressembler à celui d’un embryon humain. “Pour être prédictifs, ces modèles d’embryons doivent être bien faits, ajoute ainsi Nicolas Rivron. Nous avons beaucoup œuvré pour nous assurer que les cellules formées ressemblent véritablement aux cellules du blastocyte humain. Une fois qu’on sait qu’on a formé les bonnes cellules pour notre blastoïde, on peut modéliser l’implantation en laboratoire, en combinant des blastoïdes humains avec des cellules d’endomètre humain (ndlr, couche externe de l’utérus).”
Aujourd’hui, Nicolas Rivron s’enorgueillit de le dire: “Nous pouvons modéliser de façon très réelle le moment critique de l’implantation dans l’utérus”.
Dix ans de travaux pour arriver au médicament
Avec cette découverte, très attendue, l’équipe de scienctifiques a l’espoir de “lutter contre l’infertilité” à l’aide de médicaments, mais aussi de “proposer un nouveau modèle de contraception”. “Nous avons créé des alternatives éthiques et techniques à l’embryon humain qui permettent de comprendre les premières étapes de l’embryogenèse en laboratoire, et de développer des médicaments pour traiter les problèmes d’infertilité”, explique Nicolas Rivron.
Néanmoins, il faudra faire preuve d’un peu de patience. “Il faut encore compter une dizaine d’années de travail pour développer ce type de médicaments, précise le chercheur engagé sur la question. J’ai la conviction que ce sont des problèmes de santé globale qui ont un impact extrêmement important sur nos sociétés, sur l’égalité des genres et sur le fait de donner la possibilité aux femmes de contrôler leur fertilité.”
L’impact de ces travaux pourrait aussi prendre la forme d’un nouveau contraceptif. “Si l’implantation de l’embryon est empêchée, il ne peut y avoir de grossesse”, explique Nicolas Rivron.
Deux autres découvertes majeures
Le modèle de Nicolas Rivron est donc capable de mimer le comportement d’un blastocyte, et de s’attacher aux cellules de l’endomètre sur un côté, exactement comme le fait un blastocyte. Ainsi, les blastoïdes ont réussi à créer spontanément des cellules adhérentes qui leur permettent d’interagir avec les cellules de l’endomètre.
À ce sujet, l’équipe autrichienne de Nicolas Rivron a fait une autre découverte majeure: ces cellules adhérentes se forment grâce à des signaux chimiques produits par les cellules internes de l’embryon, celles qui vont plus tard former le corps, non pas les cellules externes, comme les scientifiques s’y attendaient.
Ainsi, c’est la partie interne de l’embryon qui instruit -chimiquement- le futur placenta, pour qu’il devienne adhérent et interagisse avec l’endomètre.
Pour Nicolas Rivron, “ces modèles d’embryons vont nous aider à comprendre tous ces aspects fondamentaux qui étaient inaccessibles jusqu’à présent”.
À voir également sur Le HuffPost: La pilule contraceptive a des effets sur votre cerveau que vous ignorez peut-être
Cet article a été initialement publié sur Le HuffPost et a été actualisé.

 Yahoo Finance
Yahoo Finance 

